Содержание.
ПОГЛОЩЕННЫЕ ДОЗЫ В МЕДИЦИНЕ
4.1 Дозы в лучевой терапии
4.2 Дозы в радионуклидной диагностике
4.3 Дозы населения от компонентов ядерной медицины
4.4 Методы снижения медицинских дозовых нагрузок на население
4.5 Дозы облучения медицинского персонала
Достоверные оценки доз ионизирующих излучений, получаемых пациентом при рентгеновской или радионуклидной диагностике, а также при лучевой терапии является весьма актуальной и достаточно сложной проблемой. В клинической практике необходимо рассчитывать разные поглощенные дозы: общую дозу, полученную пациентом, локальную дозы, полученную патологическим очагом и прилегающими к нему тканями, дозу, полученную участком кожи, через которую входит в тело излучение. Вычисления затруднены гетерогенностью объекта излучения, достаточно сложной томографии, плохой определенностью значений коэффициентов поглощения излучения в различных компонентах среды, трудностями учета рассеяния излучения различными органами и тканями. Для реальной среды, введение обоснованных параметров типа эффективного коэффициента поглощения излучения, дозового и энергетического факторов накопления, необходимых для восстановления пространственного распределения дозового поля, представляет собой весьма не простую задачу. Трудности дозиметрии связаны и с отсутствием единого алгоритма расчета для всех видов излучения: для рентгеновского, нейтронного излучения, электронов, протонов, дейтронов и т.п. требуются специальные методики вычислений. Дозиметрию приходится проводить для пациента, врача и для населения в целом.
В данной лекции мы коротко остановимся на особенностях дозиметрии в клинической практике ядерной медицины. В первой части даны классические определения экспозиционной и поглощенной дозы и единицы их измерения. Во второй части рассмотрены особенности локальной дозиметрии и методы восстановления пространственного распределения дозового поля в облучаемом гетерогенном объекте. Заключительная часть лекции посвящена оценке коллективной дозы, получаемой населением и медиками-профессионалами за счет процедур в сфере ядерной медицины.
Действие ионизирующих излучений на любое вещество проявляется в ионизации атомов и молекул, входящих в состав этого вещества. Мерой этого воздействия служит поглощенная доза - фундаментальная дозиметрическая величина, определенная как отношение поглощенной энергии излучения в единице массы. Основной единицей поглощенной энергии в системе СИ является грей (Гр, Gy) - джоуль на килограмм массы (Дж·кг-1). Обозначается она символом "D". Поглощенная доза в 1 Гр является довольно значимой радиационной величиной и может вызвать в облученном организме ряд последствий. Но в собственно энергетическом смысле эта величина очень мала - повышение температуры тела человека в результате воздействия этой дозы менее одной тысячной градуса.
При измерении эффектов, возникающих в веществах под действием ионизирующих излучений, используется понятие доза, а при оценке влияния облучения на биологические объекты поправочные коэффициенты. Повреждений, вызванных в живом организме излучением, будет тем больше, чем больше энергии оно передаст тканям; количество такой переданной организму энергии называется дозой. Дозы можно рассчитывать по-разному, с учетом того, каков размер облученного участка и где он расположен, один человек подвергся облучению или группа людей и в течение какого времени происходило.
Ведем некоторые понятия и обозначения.
Биологические эффекты - воздействие ионизирующих излучений на биологические процессы в живых организмах.
Взвешивающие коэффициенты для отдельных видов излучения при расчете эквивалентной дозы (WR) - используемые в радиационной защите множители поглощенной дозы, учитывающие относительную эффективность различных видов излучения в индуцировании биологических эффектов. Фотоны любых энергий. Электроны и ионы любых энергий. Альфа- частицы.
Взвешивающие коэффициенты для тканей и органов при расчете эффективной дозы (WТ) - множители эквивалентной дозы в органах и тканях, используемые в радиационной защите для учета различной чувствительности разных органов и тканей в возникновении стохастических эффектов радиации.
Табл. 1. Взвешивающие коэффициенты для тканей и органов при расчете эффективной дозы
| Орган или ткань | Wт |
| Гонады (яичники, семенники) | 0,20 |
| Костный мозг (красный) | 0,12 |
| Толстый кишечник | 0,12 |
| Желудок, легкие | 0,12 |
| Щитовидная железа | 0,05 |
| Печень, пищевой тракт | 0,05 |
| Кожа | 0,01 |
| Клетки костных поверхностей | 0,01 |
Для организма в целом этот коэффициент принят равным1.
Гигиеническое нормирование - установление предельных доз внешнего и внутреннего облучения, которые надежно гарантируют безопасность работающих с источниками излучения и всего населения.
Доза (от греческого - доля, порция) - энергия ионизирующего излучения (ИИ), поглощённая облучаемым веществом и часто рассчитанная на единицу его массы. Измеряется в единицах энергии, которая выделяется в веществе (поглощается веществом) при прохождении через него ионизирующего излучения.
Доза поглощенная (D) - величина энергии ионизирующего излучения, переданная веществу:
![]() ,
где dЕ - средняя энергия, переданная ионизирующим излучением веществу, находящемуся в элементарном объеме, а dm - масса вещества в этом объеме.
,
где dЕ - средняя энергия, переданная ионизирующим излучением веществу, находящемуся в элементарном объеме, а dm - масса вещества в этом объеме.
Энергия может быть усреднена по любому определенному объему, и в этом случае средняя доза будет равна полной энергии, переданной объему, деленной на массу этого объема. В единицах СИ поглощенная доза измеряется в джоулях, деленных на килограмм (Дж·кг-1), и имеет специальное название - грей (Гр). Использовавшаяся ранее внесистемная единица рад=100 эрг/г равна 0,01 Гр.
Рад - внесистемная единица поглощённой дозы. Соответствует энергии излучения 100 эрг, поглощённой веществом массой 1 грамм (сотая часть «Грэя»).
1 рад = 100 эрг/г = 0,01 Дж/кг = 0,01 Гр = 2,388·10-6 кал/г
При экспозиционной дозе в 1 рентген поглощённая доза в воздухе будет 0,85 рад (85 эрг/г).
Грэй (Гр.) - единица поглощённой дозы в системе единиц СИ. Соответствует энергии излучения в 1 Дж, поглощённой 1 кг вещества.
1 Гр. = 1 Дж/кг = 104 эрг/г = 100 рад.
Доза эквивалентная (DТ.R) - поглощенная доза, рассчитанная для биологических объектов (человек, орган, ткань), с учетом соответствующего взвешивающий коэффициент для данного вида излучения, WR: равна произведению поглощённой дозы на WR
DТ.R= D·WR,
где DT,R - средняя поглощенная доза в органе или ткани Т, а WR - взвешивающий коэффициент для излучения R.
Замечание. До недавнего времени при расчёте «эквивалентной дозы» использовались «коэффициент качества излучения» (К) и «относительная биологическая эффективность» (ОБЭ) - поправочные коэффициенты, учитывающий различное влияние на биологические объекты (различную способность повреждать ткани организма) разных излучений при одной и той же поглощённой дозе. Сейчас эти коэффициенты в Нормах радиационной безопасности (НРБ-99) названы «Взвешивающие коэффициенты для отдельных видов излучения при расчёте эквивалентной дозы (WR).
Табл.2. Взвешивающие коэффициенты для отдельных видов излучения.
| Вид излучения | Значение WR |
| Фотоны (кванты) любых энергий | 1 |
| Рентгеновское, гамма | 1 |
| Электроны (бета- частицы любых энергий), позитроны | 1 |
| Нейтроны с энергией менее 10 кэВ | 5 |
| От 10 кэВ до 100 кэВ | 10 |
| От 100 кэВ до 2 МэВ | 20 |
| От 2 МэВ до 20 МэВ | 10 |
| Более 20 МэВ | 10 |
| Протоны с энергией более 2 МэВ | 5 |
| Альфа – частицы, осколки деления, тяжёлые ядра | 20 |
При воздействии различных видов излучения с различными взвешивающими коэффициентами эквивалентная доза определяется как сумма эквивалентных доз для этих видов излучения DТ= SDТ.R
Единицей эквивалентной дозы является зиверт (Зв).
Доза экспозиционная, DE - количественная характеристика рентгеновского и гамма - излучений, определяемая по ионизации воздуха. Представляет собой суммарный электрический заряд ионов одного знака, образованных в единице объема воздуха в условиях электронного равновесия. Внесистемная единица экспозиционной дозы - рентген (Р), которой соответствует такое рентгеновское и гамма- излучение, которое образует в 1 см3 сухого воздуха (имеющего при нормальных условиях вес 0,001293 г) 2,082·109 пар ионов. Эти ионы несут заряд в 1 эл.-статическую единицу каждого знака (в системе СГСЭ), что в единицах работы и энергии (в системе СГС) составит около 0, 114 эрг поглощённой воздухом энергии (6,77·104 Мэв). (1 эрг = 10-7 Дж = 2,39·10-8 кал). При пересчёте на 1 г воздуха это составит 1,610·1012 пар ионов или 87,3 эрг/г сухого воздуха . Таким образом физический энергетический эквивалент рентгена равен 87,3 эрг/г для воздуха (для других веществ значения совершенно другие, например, для биологической ткани (воды) 95 эрг/г). В условиях электронного равновесия экспозиционной дозе 1 Р соответствует поглощенная доза в воздухе, равная 0,873 рад. Единицей измерения в системе СИ является «кулон на кг» (Кл/кг), что соответствует образованию в 1 кг воздуха такого количества ионов (6,24·1018 пар ионов), суммарный заряд которых равен 1 Кл (каждого знака). 1 кулон = 3·109 ед. СГСЭ = 0,1 ед. СГСМ. Физический эквивалент 1 Кл/кг равен 33 Дж/кг (для воздуха).
Соотношения между рентгеном и Кл/кг следующие: 1 Р = 2,58·10-4 Кл/кг - точно. 1 Кл/кг = 3,88·103 Р - приблизительно.
Доза эффективная (DE,T) - величина, используемая как мера риска возникновения отдаленных последствий облучения всего тела человека и отдельных его органов и тканей с учетом их радиочувствительности (а также веса).
Каждый орган и ткань не только по-разному реагирует на поглощенную ими дозу облучения, но и оказывает различное влияние на работу организма в целом. Для учета этих особенностей в практической дозиметрии используется понятие эффективной дозы. Эффективная (эквивалентная) ожидаемая доза учитывает суммарную радиоактивность поступающих в организм радионуклидов с учетом их периода полураспада и периода полувыведения из организма. Эффективная доза - величина, используемая как мера риска возникновения последствий, в т.ч. и отдаленных, облучения всего тела человека или отдельных его органов с учетом их радиочувствительности. Она представляет сумму произведений эквивалентной дозы в органах и тканях на соответствующие взвешивающие коэффициенты:
DE,T=DT·SWT
где DТ - эквивалентная доза в органе или ткани Т, а WТ - взвешивающий коэффициент для органа или ткани Т, т.е. множитель эквивалентной дозы в органах и тканях, используемый в радиационной защите для учёта различной чувствительности разных органов и тканей в возникновении стохастических эффектов радиации – «коэффициент радиационного риска». Чтобы учесть качественные различия излучений, их биологическая эффективность сравнивается с биологической эффективностью рентгеновского излучения, имеющего энергию кванта 250 КэВ. На практике понятие эквивалентной дозы применяют лишь для характеристики радиационных воздействий в малых дозах (не более 5 годовых ПДД для профессионалов).
Для оценки полной эффективной эквивалентной дозы, полученной человеком, рассчитывают и суммируют указанные дозы для всех органов.
Единица измерения эффективной дозы - Дж·кг-1, название – зиверт (Зв).
Бэр - биологический эквивалент рентгена (в некоторых книгах - рада). Внесистемная единица измерения эквивалентной дозы. В общем случае:
1 бэр = 1 рад К = 100 эрг/г К = 0,01 Гр К = 0,01 Дж/кг К = 0,01 Зиверт
При оценке доз в медицинской практике можно считать (с минимальной погрешностью), что экспозиционная доза в 1 рентген для биологической ткани соответствует (эквивалентна) поглощённой дозе в 1 рад и эквивалентной дозе в 1 бэр (при К=1), то есть, грубо говоря, что 1 Р, 1 рад и 1 бэр - это одно и то же.
При коэффициенте качества излучения К = 1, то есть для рентгеновского, гамма-, бета-излучений, электронов и позитронов, 1 бэр соответствует поглощённой дозе в 1 рад.
1 бэр = 1 рад = 100 эрг/г = 0,01 Гр = 0,01 Дж/кг = 0,01 Зиверт
Замечание. Зиверт – большая единица дозы: грубо говоря (для биологических объектов) 1 зиверт = 100 рентген, поэтому на практике используются меньшие единицы.
Доза эффективная (эквивалентная) годовая - сумма эффективной (эквивалентной) дозы внешнего облучения, полученной за календарный год, и ожидаемой эффективной (эквивалентной) дозы внутреннего облучения, обусловленной поступлением в организм радионуклидов за этот же год.
Единица годовой эффективной дозы - зиверт (Зв).
Доза эффективная коллективная - мера коллективного риска возникновения стохастических эффектов облучения; она равна сумме индивидуальных эффективных доз. Единица эффективной коллективной дозы - человеко-зиверт (чел.-Зв).
Зиверт - см. доза эквивалентная и эффективная
Коэффициент качества - устаревшее название взвешивающих коэффициентов для отдельных видов излучения.
Мощность дозы - доза излучения за единицу времени (секунду, минуту, час).
Нормы радиационной безопасности - разрабатываются и утверждаются на основании Закона Республики Казахстан "О санитарно-эпидемиологическом благополучии населения" и имеют обязательную силу. В настоящее время действуют Нормы радиационной безопасности (НРБ-99) СП.2.6.1.758-99.
Период полувыведения (биологический) Тб - время, за которое активность нуклида, накопленного в организме (или органе), уменьшается вдвое только вследствие процессов биологического выделения.
Период полувыведения (эффективный) Тэф - время, в течение которого активность нуклида в организме или его части уменьшается в 2 раза за счет биологического выведения и радиоактивного распада нуклида:
![]() ,
,
где Т1/2 и Тб - период полураспада нуклида (физический) и период полувыведения (биологический).
Распределение радионуклидов в организме - избирательная повышенная концентрация ряда радионуклидов в отдельных органах организма, обусловленная как химическими свойствами элементов, так и особенностями деятельности органов.
Фон - мощность экспозиционной дозы ионизирующего излучения в данном месте.
Фон естественный - мощность экспозиционной дозы ионизирующего излучения, создаваемая всеми природными источниками ИИ.
Эффекты облучения детерминированные - клинически выявляемые вредные биологические эффекты, вызванные ионизирующим излучением, в отношении которых предполагается существование порога, ниже которого эффект отсутствует, а выше - тяжесть эффекта зависит от дозы.
Эффекты облучения генетические - вызванные облучением генные лучевые повреждения в организме, которые могут привести к изменениям в организме его потомства.
Эффекты облучения канцерогенные - приводящие к возникновению злокачественных опухолей.
Эффекты излучения стохастические - вредные биологические эффекты, вызванные ионизирующим излучением, не имеющие дозового порога возникновения, вероятность возникновения которых пропорциональна дозе и для которых тяжесть проявления не зависит от дозы.
Эффекты облучения соматические - изменения в организме самого облученного индивидуума, не передающиеся потомству.
Еще раз напомним, что зиверт (Зв) - единица эквивалентной и эффективной эквивалентной доз в системе СИ. 1 Зв равен эквивалентной дозе, при которой произведение величины поглощённой дозы в Грэях (в биологической ткани) на коэффициент W будет равно 1 Дж/кг. Иными словами, это такая поглощённая доза, при которой в 1 кг вещества выделяется энергия в 1 Дж. В общем случае:
1 Зв = 1 Гр·W = 1 Дж/кг·W = 100 рад·W = 100 бэр
При W=1 (для рентгеновского, гамма-, бета-излучений, электронов и позитронов)
1 Зв соответствует поглощённой дозе в 1 Гр: 1 Зв = 1 Гр = 1 Дж/кг = 100 рад = 100 бэр.
Пример. Если в каком-либо месте зафиксирован фон (от гамма-излучения) в 25 мкР/час, то за 1 час пребывания в этом месте человек получит эквивалентную дозу (ЭД) в 0,25 мкЗв. За неделю соответственно: ЭД = 25 мкР/час · 168 час = 4200 мкбэр = 0,042 мЗв, а за год: ЭД = 25 мкР/час· 8760 час = 219000 мкбэр = 2,19 мЗв. Но если такая же поглощённая доза будет создана a-излучением (например, при внутреннем облучении), то с учётом коэффициента качества (20) эквивалентная доза за 1 час составит: ЭД = 25 мкР/час ·20 ·1 час = 5 мкЗв, т.е. она будет эквивалентна поглощённой дозе от рентгеновского, гамма-, бета-излучений, в 500 мкрад (5 мкГр).
Следует обратить внимание на резкое несоответствие между полученной дозой, т. е. выделившейся в организме энергией, и биологическим эффектом. Так давно уже стало очевидно, что одинаковые дозы, полученные человеком от внешнего и от внутреннего облучения, а также дозы, полученные от разных видов ионизирующего излучения, от разных радионуклидов (при попадании их в организм) вызывают разные эффекты! А абсолютно смертельная для человека доза в 1000 рентген в единицах тепловой энергии составляет всего 0,0024 калорий. Это количество тепловой энергии сможет нагреть только на 1oС около 0,0024 мл воды (0,0024 см3 0,0024 г), то есть всего 2,4 мг воды. Со стаканом горячего чая мы получаем в тысячи раз больше. Необходимо указывать на какой орган, часть или все тело пришлась данная доза.
Табл.3 Типы доз радиационного облучения.
|
Дозы радиационного облучения |
 |
Для наглядности, в Табл.4 собраны вместе единицы измерения активности и поглощенной дозы.
Табл.4. Единицы активности и дозы
| Единицы | |
| Беккерель (Бк, Bq) | Единица активности нуклида в радиоактивном источнике (в системе СИ). Один беккерель соответствует одному распаду в секунду для любого радионуклида |
| Грей (Гр, Gy) | Единица поглощенной дозы в системе СИ. Представляет собой количество энергии ионизирующего излучения, поглощенной единицей массы какого-либо физического тела, например тканями организма 1 Гр = 1Дж/кг |
| Зиверт (Зв,Sv) | Единица эквивалентной дозы в системе СИ. Представляет собой единицу поглощенной дозы, умноженную на коэффициент, учитывающий неодинаковую радиационную опасность для организма разных видов ионизирующего излучения. Один зиверт соответствует поглощенной дозе в 1 Дж/кг (для рентгеновского, a- и b-излучений) |
| внесистемные | |
| Кюри (Ки, Cu) | Единица активности изотопа 1 Ки = 3,700 ·1010 Бк |
| рад (рад, rad) | единица поглощенной дозы излучения 1 рад = 0,01 Гр |
| бэр (бэр, rem) | единица эквивалентной дозы 1 бэр = 0,01 Зв |
Основные радиологические величины и единицы их соотношения приведены в Табл.5.
Табл.5. Соотношения между различными единицами активности, дозы и мощности дозы.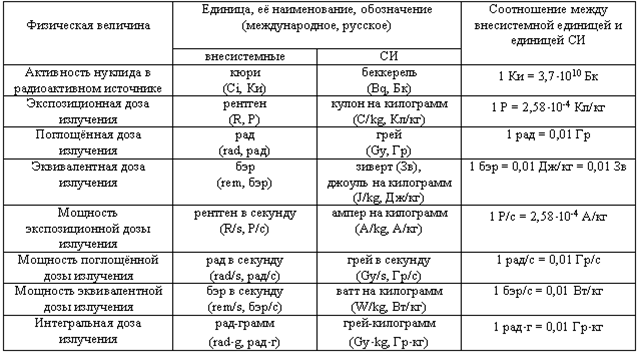
Рис.1. Коэффициенты радиационного риска.
|
Коэффициенты радиационного риска |
 |
Количество радиоактивного вещества определяется единицами радиоактивности. Бк (беккерель) - единица СИ, соответствует такому количеству радиоактивного вещества, в котором за 1 с совершается 1 распад. Распространена и внесистемная единица - кюри (Ки). Она равна 3,7 . 1010 Бк и соответствует активности 1 г 226Ra.
Имеет смысл обратить внимание на взаимосвязь относительной биологической эффективности (ОБЭ) с величиной линейной потери энергии (ЛПЭ). Так, было обнаружено, что цитостатический эффект облучения относится к функциональным лучевым реакциям; он зависит от природы излучений, следовательно, от линейной потери энергии (ЛПЭ). В прямой зависимости от величины ЛПЭ находится изменение относительной биологической эффективности. Эти соотношения, очевидно, можно связать с «эффектом насыщения», который наблюдается при радиохимических реакциях. При действии рентгеновых лучей отмечается аналогичное уменьшение выхода некоторых радиохимических реакций по сравнению с воздействием таких видов ионизирующих излучений, как нейтроны, или a-частицы, характеризующиеся высокой плотностью ионизации.
В противоположность этому при воздействии излучения с очень низкой величиной ЛПЭ (g-излучение, быстрые электроны) появляется зависимость относительной биологической эффективности от величины дозы излучения. Это имеет место также при действии одной частицы, проходящей через радиочувствительные структуры, при сравнении с эффектом многих частиц, производящих меньшую плотность ионизации («аккумуляция попаданий»). Таким образом, при определенных значениях ЛПЭ обнаруживается менее выраженная зависимость максимума цитостатического эффекта от величины дозы излучений.
При воздействии малых доз излучении наблюдается угнетение клеточного деления. При больших дозах клетки окончательно теряют способность к размножению. Временное угнетение митозов и полная стерильность не могут быть обусловлены единым механизмом, несмотря на то, что оба эти явления на первый взгляд могут показаться вполне родственными.
Величины ОБЭ могут резко отличаться даже по отношению к одним и тем же биологическим объектам, если биологическую эффективность рассматривать по отношению к различным лучевым реакциям. Относительная биологическая эффективность меняется от объекта к объекту и в некоторых случаях, например, при воздействии на определенные виды клеток в культурах тканей, при малой ЛПЭ существенно зависит от мощности дозы.
В России основными нормативными документами, регламентирующими действие ионизирующих излучений на здоровье населения, являются «Нормы радиационной безопасности» НРБ-99 и «Критерии для принятия решений по ограничению облучения населения от природных источников ионизирующих излучений» (КПР-96).
Нормы радиационной безопасности распространяются на следующие виды воздействия ионизирующих излучений на человека:
в условиях нормальной эксплуатации техногенных источников излучения;
в условиях радиационной аварии;
от природных источников излучения;
при медицинском облучении.
Требования норм, а соответственно и санитарных правил, не распространяются на источники излучения, создающие при любых условиях обращения с ними:
индивидуальную годовую эффективность дозу не более 10 мкЗв;
индивидуальную годовую эквивалентную дозу в коже не более 50 мЗв и в хрусталике глаза не более 15 мЗв;
коллективную эффективную годовую дозу не более 1 чел. Зв.
Требования норм так же не распространяются на космическое излучение на поверхности земли и внутреннее облучение человека, создаваемое природным калием - 40, на которые практически не возможно влиять.
Нормами радиационной безопасности устанавливаются основные дозовые пределы и производные от них контролируемые параметры. К основным дозовым пределам относятся: эффективная доза, эквивалентные дозы облучения хрусталика глаза, кожи, кистей и стоп за год. При оценке доз облучения персонала или населения необходимо учитывать характер облучения: при общем облучении доза сравнивается с эффективной дозой, а при местном облучении - с пределом эквивалентной дозы для облучаемой части тела. Распределение получаемой дозы в течение года не регламентируется, за исключением женщин в возрасте до 45 лет, для которых месячная доза облучения области живота не должна превышать 1 мЗв, а годовое поступление радионуклидов не должно превышать 1/20 предела годового поступления (ПГП) для персонала.
Табл.6. Значения предельно допустимых доз и некоторые официальные данные о последствиях облучения для человека.
| 2 бэр (20 мЗв) |
- предельно допустимая доза (ПДД) - наибольшее значение индивидуальной эквивалентной дозы для персонала объектов атомной промышленности, непосредственно работающего с ИИИ (категория А облучаемых лиц) за календарный год. При такой годовой дозе равномерное облучение в течение 50 лет не может вызвать в состоянии здоровья неблагоприятных изменений, обнаруживаемых современными методами. Эта доза эквивалентна тому, что человек постоянно в течение 50 лет находится (живёт) в условиях фона в 570ч 650 мкР/час. |
| 0,5 бэр (5 мЗв) | - предел дозы (ПД) - допустимая индивидуальная эквивалентная доза облучения населения, проживающего в санитарно-защитных зонах, зонах наблюдения объектов атомной промышленности (категория Б облучаемых лиц) за календарный год. При такой годовой дозе равномерное облучение в течение 70 лет не вызывает изменений в состоянии здоровья, обнаруживаемых современными методами диагностики. Исходя из этой дозы, допустимый безопасный фон 55ч 65 мкР/час (0,6 мкЗв/час). |
| 0,05 бэр (0,5 мЗв) | - по существовавшим ранее нормам годовая предельно допустимая индивидуальная эквивалентная доза для внешнего и внутреннего облучения всего населения. В настоящее время эта доза не регламентируется. Ей соответствует фон в 5-7 мкР/час (0,06 мкЗв/час). |
| 10 бэр (0,1 Зв) | - в течение года - не наблюдается каких-либо заметных изменений в тканях и органах. |
| 75 бэр (0,75 Зв) | - незначительные изменения в крови. 100 бэр (1 Зв) - нижний предел начала лучевой болезни. |
| 300-500 бэр (3-5 Зв) | - тяжёлая степень лучевой болезни, погибают 50% облучённых. |
 Эффективная доза облучения природными источниками излучения всех работников, включая персонал, не должна превышать 5 мЗв/год.При проведении профилактических медицинских обследований годовая эффективная доза не должна превышать 1 мЗв. Этот норматив может быть превышен только в случае неблагополучной эпидемиологической обстановки по решению областного здравотдела или при необходимости лечения пациента с его согласия.
Эффективная доза облучения природными источниками излучения всех работников, включая персонал, не должна превышать 5 мЗв/год.При проведении профилактических медицинских обследований годовая эффективная доза не должна превышать 1 мЗв. Этот норматив может быть превышен только в случае неблагополучной эпидемиологической обстановки по решению областного здравотдела или при необходимости лечения пациента с его согласия.
Рис.2. Летальные дозы
Перейдем теперь к другому крайнему случаю – летальным дозам. Если доза облучения достаточно велика, облученный человек погибнет. Во всяком случае, очень большие дозы облучения порядка 100 Гр вызывают настолько серьезное поражение центральной нервной системы, что смерть, как правило, наступает в течение нескольких часов или дней (Рис.2). При дозах облучения от 10 до 50 Гр при облучении всего тела поражение ЦНС может оказаться не настолько серьезным, чтобы привести к летальному исходу, однако облученный человек скорее всего все равно умрет через одну-две недели от кровоизлияний в желудочно-кишечном тракте.
При еще меньших дозах может не произойти серьезных повреждений желудочно-кишечного тракта или организм с ними справится, и тем не менее смерть может наступить через один-два месяца с момента облучения главным образом из-за разрушения клеток красного костного мозга - главного компонента кроветворной системы организма: от дозы в 3-5 Гр при облучении всего тела умирает примерно половина всех облученных.
Рассмотрим теперь важный для ядерной медицины случай – «допустимые» дозы в лучевой терапии. На Рис.3 указаны «допустимые» дозы облучения при лучевой терапии, т. е. такие дозы, которые пациент без особого вреда для себя может получить за пять сеансов в течение недели. Диаграмма дает примерное представление о том, насколько различается чувствительность к облучению разных органов и тканей организма человека.
 Рис.3 «Допустимые» дозы в лучевой терапии
Рис.3 «Допустимые» дозы в лучевой терапии
Вид преобразований в облученном веществе зависит от типа ионизирующего излучения. Поток заряженных альфа- и бета- частиц, проходя через вещество, взаимодействует, в основном, с электронами атомов и передает им свою энергию, которая расходуется на отрыв электрона от атома (ионизация) и возбуждение атома (переход одного из электронов с ближних орбит на более удаленную от ядра оболочку). При этом энергия частиц распределяется на эти два процесса примерно пополам.
Табл.7 Пробег альфа- и бета- частиц в мышечной ткани.
| Энергия частиц, МэВ | Пробег, мм | |
| a-частицы | b-частицы | |
| 0,1 | - | 0,1 |
| 0,3 | - | 0,7 |
| 0,5 | - | 1,4 |
| 0,6 | - | 1,7 |
| 1,0 | 0,003 | 3,5 |
| 1,2 | 0,004 | 4,3 |
| 2,0 | 0,01 | 8,0 |
| 2,3 | 0,012 | 9,6 |
| 3,0 | 0,015 | 12,5 |
| 3,5 | 0,02 | 14,5 |
| 5,0 | 0,05 | - |
Из таблицы видно, что если радиоактивный элемент не находится внутри организма, альфа- частицы через неповрежденную кожу практически проникнуть не могут.
Число ионизированных и возбужденных атомов, образуемых a- частицей на единице длины пути в среде, в сотни раз больше, чем у ?- частицы. Это обусловлено тем, что масса b- частицы примерно в 7000 раз больше массы a- частицы (электрона) и, следовательно, при одной и той же энергии ее скорость значительно ниже (в воздухе - порядка 20000 км/с и 220000-270000 км/с соответственно). Очевидно, что чем меньше скорость частицы, тем больше ее вероятность взаимодействия с атомами среды, следовательно, и больше потери энергии на единице пути и меньше пробег. Из Таб.7 следует, что пробег b- частиц в мышечной ткани в 1000 раз меньше, чем пробег a- частиц той же энергии. Из этой же таблицы ясно, что альфа- и бета- излучения значимый вред живому организму приносят при попадании внутрь его, а при попадании на кожу – при высокой концентрации и длительном времени воздействия.
Нейтрино, возникающие при каждом b- распаде ядра, не имеют массы покоя и заряда и со средой не взаимодействуют. Гамма- кванты, являющиеся очень высокочастотным электромагнитным излучением, производят в среде и живом организме ионизацию, в сотни раз меньшую, чем бета- частицы. Их проникающая способность, в отличие от заряженных частиц, очень велика. Принципиально по иному происходит взаимодействие нейтронов с веществом. Они взаимодействуют не с электронными оболочками атома, а с ядром, передавая ему часть энергии. Вылетевшее положительно заряженное ядро производит ионизацию среды. Кроме этого, часть нейтронов малой энергии может захватываться ядром с мгновенным излучением гамма- кванта или же с образованием новых радиоактивных элементов в облучаемой среде.
Таким образом, для любого вида ионизирующих излучений, первичными процессами, которые происходят в среде, являются ионизация и возбуждение. Поэтому биологические эффекты, наблюдаемые под воздействием заряженных частиц, нейтронов и гамма- квантов, обусловлены не их физической природой, а тем более их источником (различные естественные и техногенные радионуклиды, генераторы излучений), а количеством поглощенной энергии и ее пространственным распределением (микрогеометрией), характеризуемыми линейной плотностью ионизации. Чем выше линейная плотность ионизации или, иначе, линейная передача энергии (ЛПЭ), тем больше степень биологического повреждения. Эта степень определяет относительную биологическую эффективность (ОБЭ) различного рода излучений (см. выше).
 Человек получает радиационную дозу от различных источников. Дополнительный природный радиационный фон от космического излучения и радиоактивных материалов, находящихся в земле и внутри нашего тела, составляет примерно 30-40%. Оставшиеся 10-20% приходятся на облучение от деятельности человека, в основном это медицинские исследования при рентгенографии и радиационной терапии. Вклад от последствий ядерных взрывов, работы АЭС и ТЭС на углях количественно составляет всего 0,2-1,0% (Рис.4).
Человек получает радиационную дозу от различных источников. Дополнительный природный радиационный фон от космического излучения и радиоактивных материалов, находящихся в земле и внутри нашего тела, составляет примерно 30-40%. Оставшиеся 10-20% приходятся на облучение от деятельности человека, в основном это медицинские исследования при рентгенографии и радиационной терапии. Вклад от последствий ядерных взрывов, работы АЭС и ТЭС на углях количественно составляет всего 0,2-1,0% (Рис.4).
Рис.4. Средние мировые данные по вкладам различных источников радиации в общую дозу, получаемую среднестатистическим жителем Земли (сумма 2,7 мЗв).
Медицинские процедуры вносят существенный вклад в дозовую нагрузку на население. В качестве примера в Табл 8. приведены дозы облучения от различных источников фотонного излучения.
Табл.8. Дозы облучения от источников рентгеновского и гамма- излучения
| Вид облучения | Доза |
| Просмотр цветного телевизора первых моделей в течение 2 часов с расстояния 2 метров | 1 микрорентген |
| Просмотр того же телевизора по 3 часа в день в течение одного года | 0,5…0,7 миллирентген |
| Прием радоновой ванны | 1…100 миллирентген |
| Флюорография | 10…50 миллирентген |
| Рентгеновское обследование | 10…300 миллирентген |
| Рентгеновская томография (для компьютерной томографии в 5…50 раз меньше) | 0,5…10 рентген |
| Лучевая гамма-терапия после операции | 20…50 рентген |
В практике лучевой терапии используются дополнительные характеристики доз излучений, учитывающие основные клинические условия. Так, под понятием входная доза понимают дозу излучений, измеренную в воздухе на определенном расстоянии между источником излучения и поверхностью тела. Особый клинический интерес представляют показания о величине дозы, которая проявляет свое действие в определенных участках тканей. Такая эффективная доза с физической точки зрения определяется как величина энергии, которая поглощается в определенном участке тела. Эффективная доза, измеренная на поверхности тела, называется поверхностной дозой, а измеренная в определенных слоях ткани – глубинной (локальной). Величина поверхностной дозы определяется не только входной дозой, но также и рассеянным излучением, которое возникает в тканях. Величина поверхностной дозы зависит от природы излучений, их энергии и объема облучаемого участка тела. Объем облучаемого участка определяется величиной поля облучения и толщиной данного участка тела.
Для определения эффективной дозы в том или ином участке тела важно знать данные о пространственной, объемной и интегральной дозах, т. е. о суммарной величине энергии, поглощенной в определенном объеме тела. Терапевтическая эффективность излучений определяется в первую очередь очаговой дозой, т.е. эффективной дозой в патологическом очаге. Если ее сопоставить с дозой в облученном объеме тела, то можно получить величину относительной очаговой пространственной дозы.
Различия в распределении дозы при воздействии обычных рентгеновых лучей и корпускулярных излучений (протоны, a-частицы и др.) высокой энергии становятся особенно отчетливыми при учете относительных глубинных доз, т. е. отношения глубинной к максимальной или поверхностной дозе. При воздействии излучений высокой энергии, учитывая особенности распределения дозы, отношение глубинной к максимальной дозе выражают в виде относительной глубинной дозы. В противоположность этому при воздействии обычных рентгеновых лучей под относительной глубинной дозой чаще понимают отношение глубинной дозы к поверхностной. Сопоставление этих двух величин относительных доз вполне возможно, так как в случае применения обычных рентгеновых лучей поверхностная доза почти совпадает с максимальной.
Особенности действия корпускулярных излучений высокой энергии в тканях определяются специфическим распределением дозы каждого вида излучений, которое отличается от такового при воздействии обычных рентгеновых лучей. За исключением нейтронов, все другие виды излучений высокой энергии, в том числе протоны и дейтроны, характеризуются следующими особенностями распределения дозы по глубине облучаемого объекта: 1) увеличением относительной глубинной дозы; 2) уменьшением поверхностной дозы; 3) уменьшением объемной дозы. Увеличение относительной глубинной дозы для лучевой терапии имеет большое значение, так как патологический очаг, находящийся на большой глубине, благодаря этому может получить большую дозу излучений без одновременного увеличения поверхностной дозы. В то время как при воздействии обычных рентгеновых лучей максимум дозы лежит близко к поверхности тела и резко падает, в подлежащих тканях при применении излучении высокой энергии максимум дозы смещен в глубину тканей; при этом отмечается значительно меньшая потеря величины дозы с глубиной.
При воздействии излучений высокой энергии и быстрых электронов (по сравнению с воздействием равных доз обычных рентгеновых лучей с энергией 200 кв.) в ткани на глубине 8 см отмечается чрезвычайно выгодное для лучевой терапии распределение доз. В частности, уже при использовании современных установок для телегамматерапии - достигается значительное увеличение глубинных доз и уменьшение неблагоприятного действия излучений на кожу. Применение корпускулярных излучений по сравнению с телегамматерапией дает еще более выгодное распределение глубинных доз.
Корпускулярные излучения особенно пригодны для лечения глубоко расположенных опухолей, так как в глубоких слоях тканей при воздействии этого вида излучений создается чрезвычайно высокая относительная глубинная доза. В противоположность этому быстрые электроны с энергией от 10 до 20 Мэв в связи с особенностями распределения дозы применяются для лучевой терапии при поверхностной локализации опухолей. Быстрое падение дозы в глубине тела, которое наблюдается при воздействии электронов, положительно сказывается на относительной пространственной дозе в очаге и приводит лишь к очень незначительному облучению подлежащих здоровых тканей. Изменение величины глубинных доз в воде различных видов излучений; дозы выражены в процентах эквивалентным дозам в опухоли на глубине 8 см.
При воздействии излучений высокой энергии вследствие незначительной эффективной поверхностной дозы на входном поле нет необходимости ограничивать облучения, чтобы щадить кожу, как это приходится делать в случае применения обычных рентгеновых лучей. При воздействии излучений очень высокой энергии кожа на входном поле не подвергается переоблучению. Это же явление при облучении электронами наблюдается при диапазоне энергий от 3 до 20 Мэв. Причиной щажения кожи на входном поле является увеличение длины пробега ионизирующих частиц при возрастании их энергии. Например, если вторичные электроны с относительно малой энергией в 200 кэв вследствие своего небольшого пробега оказывают воздействие практически в тех участках, где происходит первичное поглощение квантов, то вторичные электроны высокой энергии имеют большую длину пробега. Такие вторичные электроны высокой энергии вызывают ионизацию не на месте первичного поглощения излучений, а вдоль всей траектории, причем плотность ионизации особенно велика в конце траектории. В связи с тем, что электроны движутся главным образом прямолинейно вдоль пучка излучений, место воздействия излучений перемещается в более глубокие слои тканей, соответственно длине пробега, определяемой величиной энергии электронов. Такая особенность действия излучении высокой энергии, называемая эффектом лавины или Переходным эффектом, приводит к перемещению максимума дозы в глубь тканей и поэтому величина дозы от поверхности в глубь ткани не падает, а повышается. Так, например, максимум дозы g-излучений от радиоактивного кобальта в тканях, эквивалентных по плотности воде, находится примерно на глубине 3—5 мм, а для излучений и электронов с энергией 15 Мэв - на глубине около 30 мм. Величина и характер возрастания дозы при движении вглубь облучаемого тела в значительной степени зависят от природы излучений, размера поля и расстояния источник - кожа.
Помимо локальных доз (очаговой, глубинной и поверхностной), определяющих облучение кожи, при проведении лучевой терапии особый интерес представляет доза излучения, поглощенного всем телом, т. е. объемная или интегральная доза, и сопоставление ее с величиной очаговой дозы. Значения интегральных доз для отдельных видов излучений и пространственное распределение глубинных доз могут быть рассчитаны из данных по распределению интенсивности излучений по изодозам. При сопоставлении значений интегральных доз разных видов излучений оказывается, что обычная рентгенотерапия непригодна для лечения глубоко расположенных опухолей, так как при увеличении глубины расположения опухоли интегральная доза очень резко возрастает и, следовательно, здоровые ткани при этом подвергаются интенсивному облучению. Для лечения опухолей, расположенных как поверхностно, так и на большой глубине, учитывая небольшие интегральные дозы, с успехом можно применять дистанционную гамма терапию. В противоположность этому рентгеновские излучения высоких энергий особенно пригодны для лечения глубоко расположенных опухолей, так как при таком лечении интегральная доза относительно низкая, поверхностная доза на входном поле очень мала, сохраняется узкий рабочий пучок излучения и не наблюдается существенного рассеяния излучений. В костной ткани при определенных уровнях энергий не происходит повышенного поглощения излучении.
Совершенно иная картина наблюдается при воздействии электронов. При проведении глубокой лучевой терапии при помощи электронов интегральная доза очень быстро возрастает с глубиной, что особенно заметно при сопоставлении с воздействием тормозного излучения такой же энергии. Это возрастание интегральной дозы связано с тем, что при применении электронов с энергией до 30 Мэв, необходимых для осуществления глубокой лучевой терапии, доза позади очага снижается недостаточно круто. К тому же в результате рассеяния излучений происходит «паразитическое» облучение здоровых тканей, расположенных вокруг поля облучения. Оно относительно больше при использовании малых полей. С точки зрения величины интегральной дозы лучевая терапия быстрыми электронами особенно целесообразна при поверхностно расположенных опухолях. По минимальным значениям интегральных доз электронное излучение имеет преимущества по сравнению с рентгеновыми лучами при расположении опухоли на глубине не более 6 см под поверхностью кожи, а оптимальная энергия электронов составляет не более 20 Мэв. Чрезвычайно низкая интегральная доза при облучении электронами небольшой энергии поверхностно расположенных опухолей обусловлена резко ограниченной глубиной проникновения электронов с такой энергией. Поэтому паразитического облучения здоровых тканей, расположенных за очагом, практически не наблюдается.
В принципе, облучение в медицине направлено на исцеление больного. Однако, нередко дозы оказываются неоправданно высокими: их можно было бы существенно уменьшить без снижения эффективности, например, более точная фокусировка гамма-луча, причем польза от такого уменьшения была бы весьма существенна, поскольку дозы, получаемые от облучения в медицинских целях, составляют значительную часть суммарной дозы облучения от техногенных источников.
Табл. 9. Дозы, полученные человеком на отдельные части тела
| Части тела | Череп, гортань | Шейный отдел позвоночника | Поясничный отдел позвоночника | Пояснично-крестцовый отдел позвоночника | Кости таза | Органы грудной клетки | Флюорография грудной клетки |
| прямая проекция, мЗв | 50 | 60 | 800 | 1700 | 750 | 400 | 540 |
| боковая проекция, мЗв | 30 | 300 | 1200 | 470 | 600 | 730 |
При создании дозиметрических моделей для внутренних источников радиации, в первом приближении удобно рассматривать две группы анатомических регионов в организме: группа «источников», в которых внутри тела локализована радиоактивность и группа «мишеней», включающая органы и ткани, находящиеся под облучением, для которых нужно рассчитывать поглощенную радиационную дозу. В качестве фундаментальной дозиметрической величины вводят среднюю поглощенную дозу в регионе-мишени. Основной биологический эффект, важный для радиационной защиты - индукция рака, имеет клеточную природу, и средняя доза на мишень соотносима с той дозой, которую получают клетки риска. Допускается, что клетки риска равномерно распределены в регионе-мишени. Регионы-источники отобранные для рассмотрения состоят из точно обозначенных регионов и неуточнямого региона, который называют Другой, определяемого как дополнительный к набору точно обозначенных регионов. Полагают, что радиоактивность равномерно распределена в каждом регионе-источнике. Для большинства регионов активность распределена по объему объекта, но в минеральных костных регионах и в дыхательных путях активность может быть распределена по поверхности исследуемого объекта. Для всех регионов-мишеней подходящей величиной является средняя энергия излучения, поглощенная в объеме мишени, усредненная по массе мишени.
Важно понимать, что массы регионов, как «источников», так и «мишеней» (и, следовательно, дозы), зависят от возраста человека.
Средняя поглощенная энергия в регионе-мишени зависит от природы радиации испускаемой регионами-мишенями, пространственных расположений регионов-источников и мишеней, а также от природы тканей в регионах. Эти факторы учитывают радионуклид-специфические коэффициенты, называемые эспецифическими энергиями или SE. Для любого радионуклида, органа-источника S, органа-мишени Т, специфическая энергия определяются как
|
|
(1) |
где Yi - выход излучения типа i на один акт распада, Ei - средняя или единственная энергия излучения типа i, AF(T_S;t) - доля энергии, испущенной из источника S, поглощенная мишени Т в человеке возраста t, и MT(t) - это масса мишени в возрасте человека t. Зависимость SE от возраста вытекает из возрастной зависимости поглощенной доли и массы мишени. Величина AFi(T_S; t) - поглощенная доля (AF) и, когда ее делят на массу мишени, ее называют специфической поглощенной долей (SAF).
При расчете эквивалентной дозы на регион, эффективной дозы и при оценке риска, основной величиной является уровень поглощенной дозы в разные времена. Уровень дозы в мишени Т включает вклады от каждого радионуклида в организме и от каждого региона, где присутствуют радионуклиды. Поглощенный уровень дозы в возрасте t в регионе Т у человека в возрасте t0 на момент поступления, DT(t, t0), можно выразить как
|
|
(2) |
где qs,j(t) - активность радионуклида j представленная в источнике S в возрасте t, SE (T_S; t)j есть специфическая энергия поглощенная в регионе Т на один акт распада радионуклида j в источнике S в возрасте t, а с - числовая константа зависящая от единиц q и SE.
В радионуклидной диагностике используются короткоживущие радионуклиды, поэтому учет радиоактивного распада а дозиметрии представляет собой естественную задачу. В Ур.1 есть два параметра, связанных с радиоактивным распадом: Yi - это выход радиации типа i на акт распада и Ei - средняя или единственная энергия радиации типа i. При работе с b-излучателями следует учитывать непрерывный спектр электронов. Полная форма b-спектра обычно используется только в дозиметрии дыхательного тракта. Для других органов используются только средние энергии b-распада. Полагают, что электроны полностью поглощаются в регионе-источнике. В случае изотопов, меченных a-излучателями, используют кинетические энергии каждой испускаемой альфа-частицы, и кинетической энергией ядер отдачи. Энергия атомов отдачи Er для альфа распада рассчитывается как
|
|
(3) |
где Ea - кинетическая энергия альфа-частицы, А - массовый номер нуклида, а 4.0026 - атомная масса альфа частицы.
Рис.5 Фантомы людей различного возраста и пола для расчета поглощенной дозы от внутреннего гамма излучения Гамма-радиацию с энергией фотонов ниже 10 КэВ считают непроникающей радиации для большинства очагов; она поглощается в источнике. Расчет поглощенной дозы фотонного излучения часто осуществляют на фантомах человека, представляющих новорожденного, 1, 5 и 10-тилетнего ребенка, 15-летнего мужчины и взрослого мужчины (Рис.5). Существуют и специально женские фантомы.
Использование ионизирующего излучения в медицинской практике для диагностики и лечения широко распространено в мире. Оно включает лучевую диагностику, лучевую терапию, ядерную медицину, интервенциональную радиологию. Облучение в медицинских целях занимает второе (после естественного радиационного фона) место по вкладу в облучение населения на Земном шаре. В последние годы радиационные нагрузки от медицинского использования излучения обнаруживают тенденцию к возрастанию, что отражает все большую распространенность и доступность рентгено-радиологических методов диагностики во всем мире. При этом медицинское использование ИИИ вносит самый большой вклад в антропогенное облучение. Усредненные данные облучения, обусловленные медицинским использованием излучений в развитых странах, приблизительно, эквивалентны 50% глобального среднего уровня облучения от естественных источников. Это связано, в основном, с широким применением в этих странах компьютерном рентгеновской томографии. Диагностическое облучение характеризуется довольно низкими дозами, получаемыми каждым из пациентов (типичные эффективные дозы находятся в диапазоне 1 - 10 мЗв), что в принципе вполне достаточно для получения требуемой клинической информации. Терапевтическое облучение, напротив, сопряжено с гораздо большими дозами, точно подводимыми к объему опухоли (типичные назначаемые дозы в диапазоне 20-60 Гр).
Специфика медицинского облучения состоит в том, что в интересах получения безусловной, недостижимой иным путем, пользы для больного при диагностических и терапевтических процедурах в ряде случаев приходится применять весьма высокие уровни излучения. С учетом данного обстоятельства предельные дозовые значения при медицинском облучении не устанавливаются, а ограничение уровня радиационного воздействия осуществляется с использованием принципов обоснования (по показаниям к проведению медицинских процедур) и оптимизации (применительно к мерам защиты от ИИ). При этом, в соответствии с Законом РФ "О радиационной безопасности населения" (статья 17), гражданину (пациенту) по его требованию предоставляется полная информация об ожидаемой дозе облучения и о возможных последствиях для его здоровья предлагаемой процедуры, а также право отказаться от нее (за исключением тех случаев, когда проводятся профилактические обследования в целях выявления заболеваний, опасных в эпидемиологическом отношении).
Облучение пациентов в медицине применяется с целью диагностики и лечения заболеваний. Хотя терапевтические дозы весьма велики, они не учитываются при оценке облучения населения, поскольку ожидаемая продолжительность жизни онкологических больных, как правило, значительно меньше латентного периода онкологического заболевания, которое может быть индуцировано облучением. По этой причине учитывается только доза, полученная пациентами при диагностике заболеваний. Наибольшее распространение получила рентгенодиагностика. По оценке на 1993 г., в странах с развитой рентгенодиагностикой ежегодно проводятся 320-1300 (в среднем 890) исследований на одну тысячу человек населения. Средняя доза на одно исследование составляет 1200 мкЗв/год. Вклад рентгенодиагностики в облучение населения таких стран составляет 300-2200 мкЗв/год при среднем значении 900 мкЗв/год. Радионуклидная диагностика используется значительно реже - единичные процедуры в год на одну тысячу человек. Средняя доза за одну процедуру составляет 2500 мкЗв. Вклад радионуклидной диагностики в облучение населения для стран, широко применяющих этот вид исследования, составляет 73 мкЗв/год. Для бывшего СССР эта величина составляла 32 мкЗв/год.
В годовой коллективной дозе облучения населения Российской Федерации на долю медицинского облучения приходится около 30%. Принятие Федеральных Законов Российской Федерации: «О радиационной безопасности населения» и «Санитарно-эпидемиологическом благополучии населения» принципиально изменило правовые основы организации Госсанэпиднадзора за использованием медицинских источников ионизирующего излучения (ИИИ) и потребовало полного пересмотра санитарных правил и норм, регламентирующих ограничение облучения населения и пациентов от этих источников.
Согласно НРБ-96, с целью ограничения облучения населения от медицинских источников Минздравом России устанавливаются стандартизованные контрольные уровни медицинского облучения в рентгендиагностике и рентгенотерапии, радионуклидной диагностике и терапии. Немаловажное значение имеют также совершенствование и развитие методологии радиологических медицинских процедур, создание новых, более эффективных образцов аппаратуры и оборудования.
С учетом массового характера профилактических медицинских рентгенологических процедур НРБ-96 установлен предел годовой дозы облучения, равный 1 мЗв (0,1 бэр). Его превышение допускается лишь в условиях неблагоприятной эпидемиологической обстановки, требующей проведения дополнительных исследований или вынужденного использования методов с большим дозообразованием. Решение о временном вынужденном превышении установленного предела профилактического облучения принимается управлением здравоохранения субъекта федерации.
Проведение научных исследований, связанных с облучением практически здоровых лиц, не имеющих медицинских противопоказаний, должно проводиться по решению федеральных органов здравоохранения. При этом требуется обязательное письменное согласие испытуемого и предоставление ему информации о возможных последствиях и риске исследования. Годовая доза облучения испытуемого при проведении научных исследований не должна превышать 1 мЗв (0,1 бэр).
Лица, не являющиеся работниками рентгенорадиологического отделения, но оказывающие помощь в проведении исследований (поддержке тяжелобольных пациентов, детей и т.п.) при выполнении рентгенорадиологических процедур не должны подвергаться облучению, превышающему 5 мЗв в год. Наконец, мощность дозы гамма-излучения на расстоянии 0,1 м от пациента, которому с терапевтической или диагностической целью введены радиофармацевтические препараты, не должна превышать при выходе из радиологического отделения 1 мкЗв/ч.
Строгое соблюдение требований, изложенных в Законе РФ "О радиационной безопасности населения" и НРБ-96, надежно гарантирует безопасность лиц, работающих с техногенными источниками ИИ при нормальной эксплуатации и всего населения в обычных условиях жизнедеятельности.
В России вклад медицинского облучения в интегральную дозу облучения населения особенно велик. Если средняя доза, получаемая жителем планеты, составляет 2,8 мЗв и доля медицинского облучения в ней 14%, то облучение россиян составляет 3,3 мЗв и 31,2% соответственно. В Российской Федерации 2/3 медицинского облучения приходится на рентгенодиагностические исследования и почти треть на профилактическую флюорографию, около 4% - на высокоинформативные радионуклидные исследования. Стоматологические исследования добавляют в общую дозу облучения лишь малые доли процента.
Население Российской Федерации по вкладу медицинского облучения по-прежнему является одним из самых облучаемых и, к сожалению, эта ситуация пока не имеет тенденции к снижению. Если в 1999 популяционная доза медицинского облучения населения России составляла 140 тысяч чел.-Зв, а предшествующие годы еще меньше, то в 2001 она возросла до 150 тысяч чел.-Зв. При этом численность населения страны сократилась. В России на каждого жителя в год проводится в среднем 1,3 рентгенологических исследования в год. Основной вклад в популяционную дозу вносят рентгеноскопические исследования - 34% и профилактические флюорографические исследования с использованием пленочных флюорографов - 39%.
Стратегия снижения дозовых нагрузок на население при проведении рентгенологических процедур должна предусматривать поэтапный переход в рентгенологии на технологии цифровой обработки информации и, прежде всего, при поведении профилактических процедур, доля которых в общем объеме рентгенологических исследований составляет около 33%. Расчеты показывают, что дозовые нагрузки на население при этом снизятся в 1,3 -1,5 раза.
Важным компонентом снижения дозовых нагрузок на население является правильная организация работы фотолабораторного процесса. Основными элементами его являются: подбор типа пленки в зависимости от локализации области обследования и вида рентгенологической процедуры; наличие современных технических средств обработки пленок. Использование при работе в условиях «темной комнаты» оптимального набора современных технологий позволяет за счет резкого снижения дублирования снимков и оптимизации комбинаций «экран-пленка» снизить дозовые нагрузки на пациентов на 15-25%. На современном этапе детальный анализ динамики дозовых нагрузок является основой в обосновании необходимости пересмотра медицинских технологий, использующих ИИИ, в пользу альтернативных методов исследования с оптимизацией по принципу «польза-вред». Такой подход должен быть положен в основу разработки стандартов лучевой диагностики. Большая роль в решении вышеуказанной проблемы отводится персоналу отделений лучевой диагностики. Хорошее знание используемой аппаратуры, правильный выбор режимов исследования, точное соблюдение укладок пациентов и методологии его защиты - все это необходимо для качественной диагностики с минимальным облучением, гарантирующим от брака и вынужденных повторных исследований. Общепризнанно, что именно рентгенология располагает наибольшими резервами оправданного снижения индивидуальных, коллективных и популяционных доз. Эксперты ООН подсчитали, что уменьшение доз медицинского облучения на 10%, по своему эффекту равносильно полной ликвидации всех других искусственных источников радиационного воздействия на население, включая атомную энергетику.
Для России этот потенциал значительно выше, в том числе для большинства административных территорий. Доза медицинского облучения населения страны может быть снижена примерно в 2 раза, то есть до уровня 0,5-0,6 мЗв/год, который имеют большинство индустриально развитых стран. В масштабах России это означало бы снижение коллективной дозы на многие десяти тысяч человеко-Зв ежегодно, что равносильно предотвращению каждый год нескольких тысяч смертельных раковых заболеваний, индуцируемых этим облучением. Для сравнения можно отметить, что доза облучения для населения страны от Чернобыльской аварии за 50 лет оценивается величиной не более 150 тысяч чел.-Зв, то есть равной годовой дозе медицинского облучения. Несмотря на то, что основной вклад в медицинское облучение вносит рентгенодиагностика, нельзя сбрасывать со счетов радионуклидную диагностику (РНД), тем более, что по уровню радиационного воздействия РНД отличается повышенными по сравнению с рентгенодиагностикой дозами облучения пациентов и персонала, но и большей информативностью. Практика ядерной медицины в ближайшее время будет двигаться вперед благодаря использованию новых и более избирательных радиофармпрепаратов для диагностики и терапии. Будет возрастать потребность в лучевой терапии рака.
В настоящее время правовые отношения, связанные с обеспечением безопасности населения при рентгенорадиологических исследованиях изложены более чем в 40 нормативно-правовых и организационно-распорядительных документах. Поскольку уровни облучения пациентов в медицинской практике не нормируются, соблюдение их радиационной безопасности должно обеспечиваться за счет соблюдения следующих основных требований:
проведение рентгенорадиологических исследований только по строгим медицинским показаниям с учетом возможности проведения альтернативных исследований;
осуществление мероприятий по соблюдению действующих норм и правил при проведении исследований;
проведение комплекса мер по радиационной защите пациентов направленных на получение максимальной диагностической информации при минимальных дозах облучения.
При этом должен в полном объеме осуществляться производственный контроль и государственный санитарно-эпидемиологический надзор. Реализация в полном объеме предложений госсанэпидслужбы России по оптимизации дозовых нагрузок при проведении рентгенодиагностических процедур по итогам ежегодной радиационно-гигиенической паспортизации медицинских учреждений позволит уже в ближайшие 2-3 года снизить эффективную среднюю годовую дозу облучения на одного человека до 0,6 мЗв. При этом суммарная годовая коллективная эффективная доза облучения населения уменьшится почти на 31 000 чел.-Зв, а число вероятных случаев возникновения злокачественных заболеваний (смертельных и несмертельных) снизится за этот период более чем на 2200.
При проведении рентгенорадиологических процедур облучению подвергается и сам персонал. Многочисленные опубликованные данные показывают, что в настоящее время рентгенолог получает в год дозу профессионального облучения, в среднем, около 1 мЗв в год, что в 20 раз ниже установленного предела дозы и не влечет за собой сколько-нибудь заметного индивидуального риска. Следует отметить, что наибольшему облучению могут подвергаться даже не работники рентгеновских отделений, а врачи так называемых «смежных» профессий: хирурги, анестезиологи, урологи, участвующие в проведении рентгенохирургических операций под рентгеновским контролем.
В радиобиологических экспериментах на клеточном и молекулярном уровнях показана возможность даже единичных актов ионизации вызвать нарушение некоторых наследственных механизмов. Кроме того, нельзя исключить вероятности возникновения нарушений в клеточных структурах при малых дозах облучения и соматико-стохастических и генетических эффектов, обусловленных этими нарушениями. При отсутствии прямых доказательств влияния облучения в малых дозах или, напротив, безвредности такого облучения и с учетом необходимости осторожного, гуманного подхода к нормированию радиационного воздействия при выработке норм радиационной безопасности, была предложена гипотеза об отсутствии порога для стохастических эффектов облучения и о линейной зависимости между дозой и эффектом в области малых доз. Эта гипотеза в виде официальной концепции принята Международным комитетом по радиационной защите МКРЗ и Научным комитетом по действию атомной радиации ООН (НКДАР ООН) за основу при оценке и прогнозировании ущерба от использования ионизирующего излучения и для осуществления практических разработок в области радиационной защиты. Чаще всего эту гипотезу называют концепцией беспороговой линейной зависимости доза-эффект.
Соответствующие коэффициенты линейной связи между дозой облучения и различными стохастическими (случайными) эффектами устанавливают на основе известных данных о случаях смерти в результате возникновения злокачественных опухолей и генетических дефектов в первых двух поколениях потомства облученных лиц при больших дозах. Как правило, эти коэффициенты отражают в ожидаемое число случаев n смерти от злокачественных опухолей и генетических дефектов, отнесенные к коллективной дозе 104 чел. Зв. Кроме того, при оценках воздействия излучения часто используют коэффициент риска r, равный средней индивидуальной вероятности смерти в результате облучения, отнесенной к дозе 1 Зв. Между коэффициентом риска r и ожидаемым числом случаев n смерти существует простая связь:
n= r·104
Здесь r = Зв-1; n = число случаев/104 чел. Зв.
В Табл. 10 приведены значения коэффициентов индивидуального риска возникновения смертельного заболевания злокачественными опухолями или наследственных дефектов в результате облучения тела или отдельных органов дозой 1Зв, принятые МКРЗ в 1977 и 1990 гг.
Табл. 10. Коэффициенты риска, принятые МКРЗ в 1990 в сравнении с коэффициентами 1977.
| Орган или ткань | Смертельный риск, 2·10-2, Зв-1 | |
| МКРЗ, 1977г | МКРЗ, 1990г | |
| Мочевой пузырь | - | 0,30 |
| Костный мозг | 0,20 | 0,50 |
| Поверхность кости | 0,05 | 0,05 |
| Грудные железы | 0,25 | 0,20 |
| Толстая кишка | - | 0,85 |
| Печень | 0,20 | 0,15 |
| Легкие | 0,20 | 0,85 |
| Пищевод | - | 0,30 |
| Яичники | - | 0,10 |
| Кожа | - | 0,02 |
| Желудок | - | 1,10 |
| Щитовидная железа | 0,05 | 0,08 |
| ИТОГО | 0,30 | 0,50 |
| Наследственные дефекты | 0,40* | 1,00** |
* В двух первых поколениях, ** Во всех поколениях
Риск заболевания смертельным раком при облучении всего тела составляет 5·10-2 Зв-1 (в 1972 было принято 1,25·10-2 Зв-1) для популяции, включающей людей всех возрастов. Для работающих, т.е. людей в возрасте от 18 до 65 лет, составляющий риск равен 4·10-2 Зв-1.
Если известна полученная доза, Е, риск возникновения смертельного заболевания в дальнейшей жизни человека, составляет R = 5·10-2·E
Что касается наследственных дефектов, то МКРЗ рекомендует использовать величину 1·10-2 Зв-1 для популяции всех возрастов и 0,6·10-2 Зв-1 для работающих, поскольку имеются различия в возрастном распределении. На основе этих данных МКРЗ рекомендовано установить для профессионального облучения осредненных за пять лет дозовый пробел в 20 мЗв/год, для отдельных лиц из населения – 1мЗв/год. Методики МКРЗ позволяет по определенной процедуре определять и риск не смертельных онкологических заболеваний.
Следует отдавать себе отчет в том, что при облучении малыми дозами небольших контингентов людей существующий риск появления эффектов ничтожен, а выявление таких эффектов на фоне спонтанной заболеваемости нереально. В биологии вероятность проявления эффекта менее 0,05 считается незначащей. Отсюда можно рассчитать коллективную дозу, при которой с вероятностью не менее 95% не возникает ни одного дополнительного случая рака. Такую коллективную дозу при желании можно назвать условным порогом коллективной дозы. Это позволяет в указанном смысле говорить об условном пороге коллективной дозы, обязательно с указанием вероятности проявления эффекта.
Табл.11. Реакция организма человека на интенсивное однократное облучение
| Степень лучевой болезни | Эквивалентная доза, Зв | Первичная реакция | Скрытый период | Разгар болезни | Исход болезни |
| Легкая | 1-2 | Продолжительность 1-3 дня. Слабость, головная боль, тошнота, рвота | Продолжительность 3-5 недель. Состояние вполне удовлетворительное | Состояние удовлетворительное. Слабость, головная боль, тошнота | Выздоровление через 1-2 мес., полное восстановление состава крови - через 2-4 мес. |
| Средняя | 1,5-3 | То же; эмоциональное возбуждение, переходящее в депрессию | Продолжительность 2-3 недели. Состояние удовлетворительное, но отмечается слабость, бессонница | Продолжительность 2-3 недели. Общая слабость, бессонница, повышение температуры до 380С, кожные кровотечения, инфекционные осложнения | Выздоровление через 2-3 месяца, восстановление крови через 3-5мес. В результате осложнений может быть смертельный исход |
| Тяжелая | 3-6 | Продолжительность2-4 суток. Через 10-60 минут многократная неукротимая рвота в течение 4-8часов, резкая слабость, жажда, расстройство желудка, повышение температуры 39oС. | Продолжительность до 10 суток. Слабость, бессонница, головная боль | Продолжительность 2-3 недели. Состояние тяжелое, озноб, температура до 400С, кровоизлияния и кровотечения, истощение, инфекционные септические осложнения | Выздоровление возможно при своевременном лечении через 5-10месяцев. При осложнениях смерть наступает через 10-35 суток |
| Крайне тяжелая | Свыше 6-7 | Через 10-15 минут неукротимая рвота в течение 5-6 часов, затемнение сознания, понос, высокая температура | Отсутствует | Усиление первичных реакций, непроходимость кишечника, перитонит, нарушение водно-солевого обмена. | Смерть через 5-10 суток |
| Очень высокая | Смерть наступает во время облучения |